
La biotecnología en el sector textil (primera parte).
Biotechnology in the textile sector.
Instituto Tecnológico Superior de Irapuato.
Por: Raul Ricardo Diaz Contreras.
Se presentan las generalidades y principios teóricos que rigen la acción de las enzimas en cualquier proceso, incluidos los textiles, como parte de la biotecnología y se describen ejemplos específicos en los que se emplean las enzimas en el área textil, constituyendo una gama amplia de posibilidades biotecnológicas en este sector.
Los procesos bioquímicos se han utilizado desde hace muchos años en el sector textil sin conciencia plena de los mecanismos que las biomoléculas utilizan para la conversión y transformación del sustrato sobre el que actúan, como lo pueden ser los mismos materiales y géneros usados en la industria textil. Se podrían citar muchos ejemplos: el enriado del lino, que los egipcios utilizaban para separar la parte leñosa del tallo, de los haces de fibras utilizables para obtener el hilo; procesos fermentativos para deslanado de pieles de cordero (denominado “estufado”); aplicación de enzimas en diversos procesos industriales textiles, tales como el desencolado, lavado, estampado y otros.
En esta primera parte, se revisa la utilización de enzimas y en una segunda parte se tratarán otras aplicaciones de la biotecnología en el campo textil, algunas de las cuales se observan en la Tabla 1. Aplicaciones de la biotecnología en los textiles.
La utilización de las enzimas constituye uno de los campos de la biotecnología de mayor actualidad en la industria textil, poco explorados y que podría representar un vector de gran importancia benéfica para los aspectos medioambientales por la biodegradabilidad de estos compuestos por su propia naturaleza biológica.
Conceptualmente las enzimas son un tipo de proteínas que catalizan reacciones, originalmente bioquímicas, principalmente en procesos metabólicos. Se han identificado más de 3000 enzimas diferentes.
| Aplicaciones de la biotecnología en los textiles | |
|---|---|
| Procesos enzimáticos | |
| Materias primas nuevas o modificadas | |
| Identificación y análisis de fibras | |
| Tratamiento de efluentes | |
| Biotecnología en la fabricación de auxiliares químicos textiles | |
Tabla 1. Aplicaciones de la biotecnología en los textiles.
La Comisión de Enzimas de la Unión Internacional de Bioquímica (IUB), implementó un sistema de clasificación de enzimas asignando códigos numéricos basados en la reacción catalizada, con el prefijo ‘EC’; hoy en día, es ampliamente aceptada y usada. Contiene cuatro elementos separados por puntos:
| Ejemplo. EC 4.2.1.22 | |||
|---|---|---|---|
4 |
2 |
1 |
22 |
Clase (una de las seis principales divisiones) |
Subclase |
Sub-sub-Clase |
Numero de serie de la enzima en la sub-subclase |
De manera real y como ejemplo, se presenta la Tabla 2. Clasificación de enzimas según la UIB , aplicado a las enzimas debidamente clasificadas mediante este sistema.
| Sistema de la UIB para clasificar enzimas | ||
|---|---|---|
Clase |
Subclase |
Nombre común |
1.- Oxidoreductasas |
(Grupo sobre el que actúan) 1.1 –CH–OH |
Deshidrogenasa |
1.2 –C=O |
||
1.3 –CH=CH– |
||
1.4 –CH–NH2 |
Deaminante |
|
1.5 –CH–NH |
||
1.6 NADH, NADPH |
||
1.9 HEMO |
Citocromooxidasa |
|
2.- Transferasa |
(Grupo que transfiere) 2.1 Un atomo de carbono |
|
2.2 Aldehidico o cetonico |
||
2.3 Acilo |
Colinaciltransferasa |
|
2.4 Glucosilo |
Fosforilasa |
|
2.7 Fosfato |
Hexokinasa |
|
2.8 Azufre |
||
3.- Hidrolasas |
(Enlaces que hidrolizan) |
|
3.1 Ester |
||
3.2 Glucosidicos |
||
3.4 Peptidicos |
||
3.5 Anhidridos de acido |
||
Tabla 2. Clasificación de enzimas según la UIB (solo aparecen 3 de las 6 clases).
El mecanismo general de acción enzimática se describe en la siguiente ecuación (1):
[E] + [S] ↔ [ES] ↔ [P] + [E] (1)
Donde:
E = Enzima
S = Sustrato
ES = Complejo enzima-sustrato
P = Producto
[ ] = concentración molar
Dicho mecanismo obedece la cinética de Michaelis-Menten (ecuación 2) y precisamente este conocimiento es poco aplicado en beneficio del proceso textil en el que intervienen las enzimas.
Básicamente consiste en:
(ecuación 2)
Donde:
v = velocidad de reacción
vMAX = velocidad máxima
[E] = Concentración molar de la Enzima
[S] = Concentración molar del Sustrato
KM = Constante de Michaelis-Menten
El estudio que de esto puede derivarse es realmente amplio y de gran aplicación, por ejemplo, Cavaco-Paulo y Almeida han calculado las constantes cinéticas de la reacción entre dos tipos de celulas, de las que se encuentran algunas en la Tabla 3. Constantes de velocidad de reacción.
| Tipo de proceso | Kc (mg/ml) |
|---|---|
TCLMM |
1.7 ± 0.4 |
TCHMM |
5.1 ± 1.3 |
AGLMM |
1.0 ± 0.2 |
AGHMM |
0.7 ± 0.2 |
TCLMO |
0.3 ± 0.1 |
TCHMO |
1.0 ± 0.4 |
TC = Celulasa total; AG = Celulasa Cx; LM = baja agitación; HM = elevada agitación; O = tejido original; M = tejido mercerizado. |
|
Tabla 3. Constantes de velocidad de reacción.
Inicialmente se pensaba que la actividad de las enzimas solo se realizaba en las células intactas (de ahí su nombre: ‘en-zima’= en- levadura), sin embargo ya se sabe que la mayoría de las enzimas pueden ser separadas de ellas sin perder su actividad catalítica y que además, su acción es muy específica afectando solamente al sustrato. La enzima tiene ‘centros activos’ que coinciden plenamente, como piezas de rompecabezas, con el sustrato (modelo de la llave-cerradura, v. Figura1. Modelo de la “llave-cerradura” de una enzima) sobre el que actúa (en nuestro caso algún material textil), formando un complejo intermediario (ecuación 1), logrando así disminuir la energía de activación de la reacción correspondiente, tal como se observa en la Figura 2. Disminución energía de activación por acción enzimática.
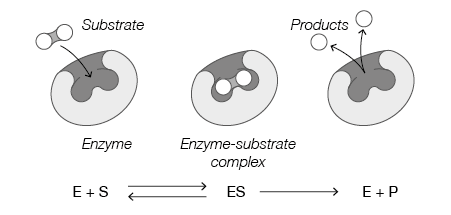
Figura 1. Modelo de la ‘llave-cerradura’, de una enzima.
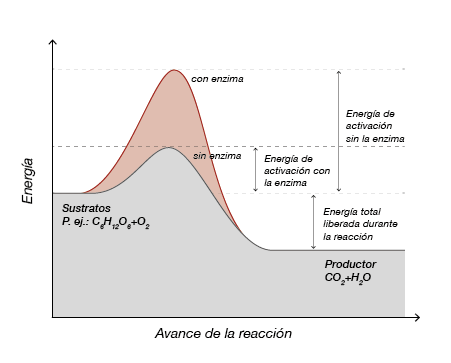
Figura 2. Disminución energía de activación por acción enzimática.
Como cualquier catalizador, las enzimas no se ‘consumen’ y son efectivas, sin embargo, pueden desnaturalizarse por ácidos o cierta temperatura.
• Macerado del lino: es un proceso fermentativo mediante el cual se descomponen las materias resinosas del tallo y así facilitar su separación por procesos mecánicos. También se le denomina ‘enriado’ ya que esta operación se hacía en los ríos con elevado coste de manipulación y contaminación. En este proceso intervienen las pectinasas.
• Lavado de la lana: este proceso elimina los aceites y grasas contenidos en la lana. En general, se utilizan lipasas.
• Deslanado biológico: el proceso tradicional de obtención de la lana de pieles consiste en tratar la piel por el lado de la carne con una solución de sulfuro sódico y cal apagada. Este método además de perjudicar a las fibras de lana, es muy contaminante. Es posible utilizar proteasas que debilitan únicamente el folículo piloso y extraer fácilmente la fibra por medios mecánicos.
• Carbonizado de la lana: para la eliminación de impurezas vegetales de la lana se realiza mediante un tratamiento ácido seguido de secado y prensado, lo que provoca perdida de afinidad tintórea y otras consecuencias mecánicas. Ha habido propuestas para que un coctel de enzimas (Biocarbo) sea utilizado en sustitución del método químico.
• Blanqueo de la lana: se propone utilizar enzimas estables en agua oxigenada.
• Desengomado o descrudado de la seda: consiste en eliminar la sericina, uno de los dos filamentos de la hebra de la seda, para dejar solamente la fibroina, mediante enzimas proteasas.
• Desencolado: aunque el uso de enzimas en este rubro ya tiene tiempo, haremos mención ya que definitivamente resulta una alternativa a los tratamientos ácidos, alcalinos o agentes oxidantes, dichas enzimas son las amilasas.
• Descrudado y blanqueo de fibras celulósicas: en la etapa de preparación del algodón, se debe someter a un proceso denominado descrude consistente en eliminar las impurezas (pectinas, ceras, pigmentos), lo cual se consigue tradicionalmente mediante descrudados alcalinos. Para esto, se propone la acción de un sistema enzimático.
Por otro lado, los restos de peróxido utilizado en el blanqueo de fibras celulósicas, pueden afectar la etapa del teñido donde se utilizan colorantes, por lo que las enzimas catalasas son una buena alternativa a la utilización de agentes reductores, además de peroxidasas, oxido-reductasas, y otras.
A continuación se muestra la reacción de una peroxidasa específica en su acción para descomponer el peróxido de hidrogeno en fibras celulósicas banqueadas antes de la tintura:
2 H2O2 + catalasa → catalasa + O2 + H2
• Lavado a la piedra (Biostoning): proceso de efecto de ‘deslavado’ de prendas de mezclilla (algodón), denominado “denim”, se realizaba de forma convencional utilizando piedras pómez abrasivas. El colorante índigo que penetra poco y queda en la superficie de las fibras e hilados, es fácilmente eliminado de las zonas de mayor roce con la piedra, dando la impresión de prendas usadas, que se ha puesto de moda; este mismo efecto, se consigue con enzimas celulasas que actúan ‘cortando’ las fibras superficiales teñidas del algodón y además con ventajas tales como: se reducen los tiempos de proceso, se causa menor daño al tejido, menor variabilidad en el aspecto, consideración al medio ambiente.
• Biopulido de fibras celulósicas: este es un tratamiento que utiliza celulasas para eliminar las microfibrillas superficiales en fibras celulósicas proporcionando superficies más limpias, suaves y con cierto efecto en consecuencia de mayor luminosidad.
• Lavado doméstico de textiles: los fabricantes de detergentes domésticos han empleado desde hace muchas décadas cocteles de enzimas para eliminar los diferentes tipos de suciedades:
a) Proteasas alcalinas, para eliminar manchas de proteínas (huevo, sangre) y sudor.
b) Lipasas, eliminan pintalabios, mantequilla, aceite y salsas.
c) Celulasas, antes citadas.
d) Amilasas, eliminan restos de espaguetis, natillas y chocolate.
A partir del conocimiento del mecanismo general de acción de las enzimas, se puede observar la gran posibilidad de aplicación que se tiene en el sector textil. Aunque en muchos procesos industriales textiles se han venido utilizando las enzimas, todavía es posible explorar y expandir su utilización para garantizar el uso de tecnologías limpias en el sector textil mediante sustancias naturales, biodegradables, que aporten beneficios para un medio ambiente más sustentable a través de estos biocatalizadores.
Briera M. M., y Nubiola J., >(1998), ‘Biotecnologia:…..’, parte I, Revista de la ind. Textil, no. 359, 70-79.
Cavaco-Paulo; y Gubitz G.M., (2003), ‘Textile processing with enzymes’, The textile Institute, Woodhead Publishing Limited, Cambridge, England.
Cegarra J., (1996), J. Soc. Dyers Col., vol 112, 327.
Diaz C. Raul R., (2001), Biopreparacion: la nueva y avanzada forma de preparar hilo y tela (primera parte), Revista Latinoamericana de Tecnologia Textil, 14, 55-60.
Lange N.K., (2000), ‘Biopreparation in action’ Int. Dyer, 185 (2), 18-21.
Lehninger A., (1975), Biochemistry, 2th edition, New York, Worth Publishers.
Stryer L., (2002), Biochemistry, 5th edition, New York, W. H. Freeman.
Sitios web:
www.expasy.ch/
www.ebi.ac.uk/swissprot/
www.rcsb.org/pdb/
